Tutkimukset
On kiehtovaa miten keho ja sen mekanismit toimii ja siksi tieteellinen- ja kokemuksellinen näyttö on erityisen tärkeää, eikä tehdä vain fiiliksen ja uskon varassa asioita, vaan aidosti mitattujen tulosten.
Lisään tänne kiinnostavia:
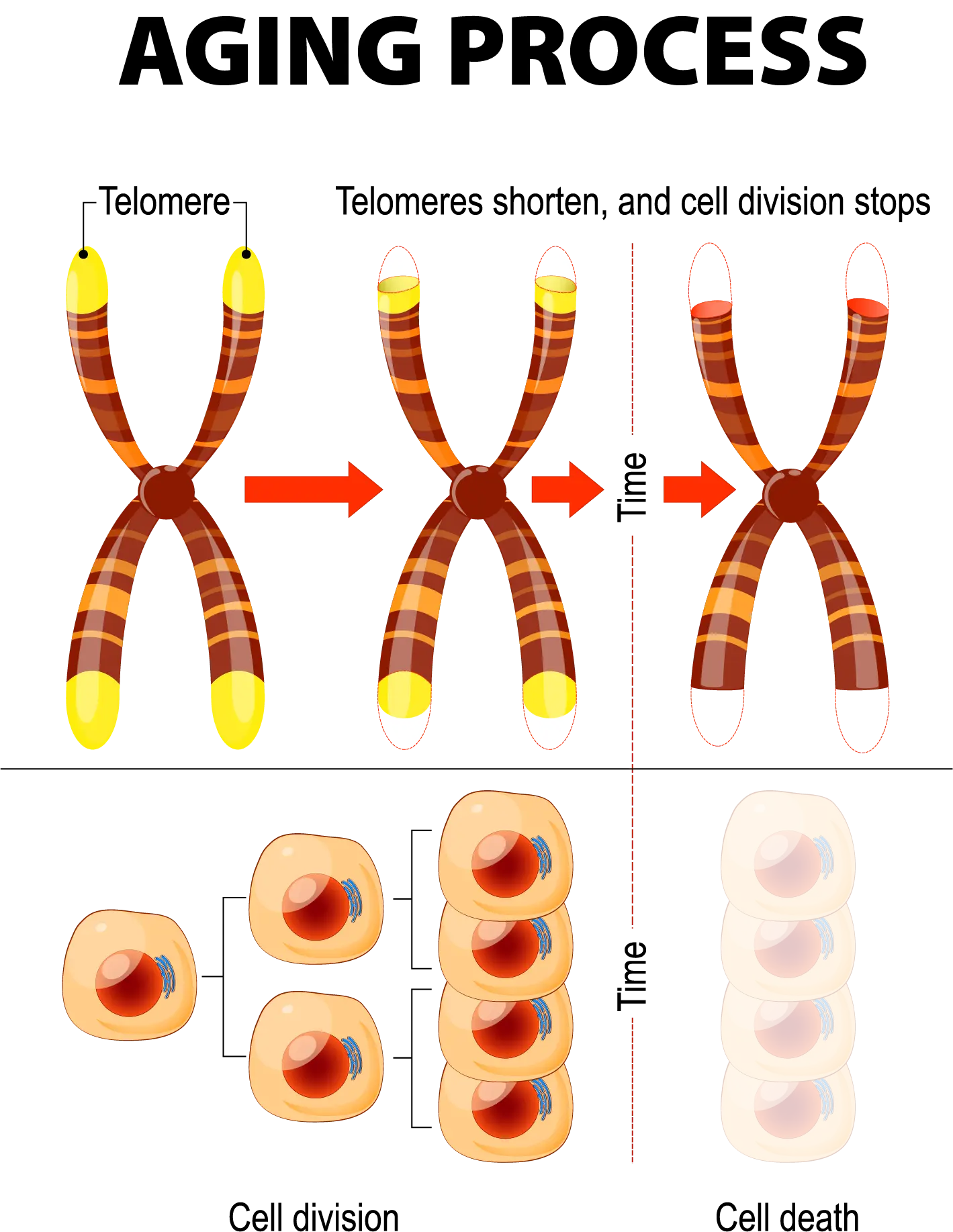
Telomeerit, solujen ikääntyminen ja mHBOT
Tutkimustausta
Hyperbaarisen happihoidon (HBOT) ja telomeeripituuden välistä yhteyttä koskeva ihmistutkimusnäyttö perustuu toistaiseksi pääasiassa valkosoluista (leukosyytit) tehtyihin mittauksiin. Merkittävin viitattu tutkimus julkaistiin vuonna 2020, ja se toteutettiin kontrolloidulla HBOT-protokollalla (Tel Aviv University).
Tutkimuksessa havaittiin:
-telomeerien pitenemistä perifeerisen veren valkosoluissa
-samanaikainen senesenttien (toiminnallisesti ikääntyneiden) solujen osuuden väheneminen
Kyseessä oli mitattava biologinen muutos, ei subjektiivinen kokemusperäinen havainto.
Miksi vaikutus havaittiin juuri valkosoluissa
Valkosolut soveltuvat telomeeritutkimukseen erityisen hyvin, koska ne:
-jakautuvat aktiivisesti
-altistuvat jatkuvasti oksidatiiviselle ja metaboliselle kuormitukselle
-heijastavat herkästi elimistön kokonaistilaa (tulehdus, stressi, palautuminen)
Näiden ominaisuuksien vuoksi valkosolujen telomeerit:
-lyhenevät nopeasti epäedullisissa olosuhteissa
-mutta voivat myös reagoida suhteellisen nopeasti, kun solun ympäristö muuttuu korjaavammaksi
Voidaanko tulosta yleistää muihin solutyyppeihin?
Suoraa yleistystä ei voida tehdä, eikä sitä tule tehdä vastuullisessa viestinnässä. Sen sijaan biologisesti perusteltu tulkinta on seuraava:
-Kaikki solutyypit eivät reagoi telomeeritasolla
-Osa soluista reagoi hitaammin tai epäsuoremmin
-Osa hyötyy ilman mitattavaa telomeeripituuden muutosta
Todennäköisesti samansuuntaisesti reagoivat solut
Kantasolut ja progenitorisolut
-erityisesti hematopoieettiset kantasolut
-telomeraasin aktiivisuus olemassa
-korkea energiariippuvuus
On biologisesti loogista, että samat olosuhteet, jotka vaikuttavat valkosoluihin, vaikuttavat myös näihin solupopulaatioihin, mutta:
-vaikutus ilmenee hitaammin
-mittaaminen ihmisellä on merkittävästi haastavampaa
Endoteelisolut
keskeisiä kudosten hapetuksen ja mikroverenkierron kannalta
telomeeripituuden sijaan vaste näkyy todennäköisemmin:
-vähentyneenä solusenenssinä
-parantuneena toiminnallisena kapasiteettina
Solutyypit, joissa telomeerivaste ei ole keskeinen
Hermosolut ja sydänlihassolut
-eivät käytännössä jakaudu
-telomeerien pituus ei ole niiden toiminnan rajoittava tekijä
Näissä soluissa mahdolliset hyödyt liittyvät:
-mitokondrioiden toimintaan
-energian tuotantoon
-solunsisäiseen viestintään
Ei telomeeripituuteen.
Mekanistinen tulkinta mHBOT:n roolista
Telomeerimuutosten ei katsota johtuvan suorasta hapen vaikutuksesta,
vaan todennäköisemmin:
-hyperoksinen–hypoksinen paradoksi
-mitokondrioiden tehostunut toiminta
-parantunut ATP:n saatavuus
-DNA:n korjausmekanismien aktivoituminen
-kroonisen matala-asteisen kuormituksen väheneminen
Toisin sanoen:
mHBOT ei "pidennä telomeerejä", vaan voi luoda soluille olosuhteet, joissa niiden omat korjausmekanismit toimivat tehokkaammin.
Yhteenveto
-Telomeeripiteneminen on osoitettu ihmisellä valkosoluissa kontrolloidussa HBOT-protokollassa
-Tulosta ei tule yleistää kaikkiin solutyyppeihin
-Osa soluista reagoi telomeeritasolla, osa toiminnallisesti
-mHBOT:n rooli on olosuhteiden optimointi, ei yksittäinen anti-aging-interventio
Näissä tutkimuksissa käsitellään fysiologisia mekanismeja (kuten hapen osapaine, mitokondrioiden toiminta ja solujen antioksidanttireitit). Ne eivät viittaa yksittäisten sairauksien hoitoon, vaan kuvaavat yleisiä biologisia ilmiöitä, joiden kautta miedon ylipainehappihoidon vaikutuksia ymmärretään.
📚 Lähteitä ja tutkimusviitteitä (tieteelliset mekanismit)
Hapen fysiologia ja kudoshapetus
-
Jain KK. Textbook of Hyperbaric Medicine. Springer.
– Klassinen teos, joka kuvaa painehappihoidon vaikutukset kudoshapetukseen ja solujen bioenergetiikkaan. -
Bosco G et al. "Mechanisms of action of hyperbaric oxygen therapy." Journal of Applied Physiology.
– Kuvaa hapen osapaineen nousun vaikutuksia solujen energiantuotantoon.
Mitokondrioiden energiantuotanto ja PGC-1α-biogeneesi
-
Hood DA. "PGC-1α as a regulator of mitochondrial biogenesis in skeletal muscle." Journal of Physiology.
– Selittää PGC-1α-reitin roolin energiantuotannon parantamisessa. -
Liang H & Ward WF. "PGC-1α: a key regulator of mitochondrial biogenesis." Cell Biology International.
Hormeettinen vaste ja Nrf2-antioksidanttireitti
-
Zhang DD. "Mechanistic studies of the Nrf2-Keap1 signaling pathway." Free Radical Biology & Medicine.
– Perusteos Nrf2-antioksidanttireitin aktivoitumisesta ja vaikutuksista solujen redox-tasapainoon. -
Calabrese EJ. "Hormesis: from cells to organisms." Critical Reviews in Toxicology.
– Esittelee hormesis-ilmiön, johon osa mHBOT:n hyödyistä perustuu.
Mitofagia, fuusio/fissio ja mitokondrioiden laatu
-
Youle RJ & van der Bliek AM. "Mitochondrial fission, fusion, and stress." Science.
– Erittäin viitattu katsaus mitokondrioiden uusiutumisesta ja laadunvalvonnasta. -
Pickles S et al. "Mitophagy and quality control." Nature Reviews Molecular Cell Biology.
– Kuvaa, miten solut poistavat vaurioituneita mitokondrioita ja miten tämä tukee kudosten toimintaa.
Anti-inflammatoriset mekanismit (NF-κB ja sytokiinit)
-
Lawrence T. "The nuclear factor NF-κB pathway in inflammation." Cold Spring Harbor Perspectives in Biology.
– Perusteksti NF-κB-reitin roolista matala-asteisessa tulehduksessa. -
Thom SR. "Oxidative stress is fundamental to hyperbaric oxygen therapy." Journal of Applied Physiology.
– Kuvaa hapen aikaansaamaa kontrolloitua oksidatiivista signaalia ja tulehdusta hillitseviä mekanismeja.
HIF-1α, angiogeneesi ja mikroverenkierto
-
Semenza GL. "Hypoxia-inducible factor 1 (HIF-1) pathway." Annual Review of Cell and Developmental Biology.
– Klassikkoviite hapenpaineen vaihtelun vaikutuksista HIF-1-signaalointiin. -
Sheikh AY et al. "Hyperoxia and angiogenesis." Journal of Clinical Investigation.
– Kuvaa hapen vaikutuksia verisuonten kasvuun ja kudosten hapensaantiin.
Yleiskatsaukset hyperbaarisen hapen vaikutuksista solubiologiaan
-
Efrati S & Ben-Jacob E. "Reflections on the neurotherapeutic effects of hyperbaric oxygen." Neuroscience & Biobehavioral Reviews.
– Laaja katsaus solubiologisista mekanismeista ja hermoston toiminnan tukemisesta. -
Heyboer M et al. "Hyperbaric oxygen therapy: current trends and mechanisms." Yale Journal of Biology and Medicine.
– Selkeä ja moderni katsaus HBOT:n fysiologisiin vaikutuksiin.
Useissa pienissä tutkimuksissa (esim. Nisa et al. 2022 & 2023, 1.4 ATA, 35–40 % O₂) on havaittu, että:
-
yhden hoitokerran jälkeen NK-solujen aktiivisuus ja määrä veressä kasvaa,
-
samalla stressihormonitasot laskevat ja parasympaattinen (rauhoittava) hermosto aktivoituu,
-
tulehdusmerkit eivät nouse, eli vaikutus ei näytä "ärsyttävältä" vaan pikemminkin palauttavalta
Termi
Tarkoitus
Merkitys mHBOT:ssa
NK-solut (Natural Killer)
Immuunijärjestelmän tappajasoluja, tuhoavat infektoituneita ja kasvaimia. Määrä ja aktiivisuus voivat lisääntyä miedon paineen happihoidon jälkeen
Parasympaattinen hermosto
Kehon "rauhoitusjärjestelmä"
Aktivoituu HBOT:ssa → sykevälivaihtelu ↑, stressitaso ↓
Redox/ROS-vaste
Solujen hapetus-pelkistystasapainon muutos
Maltillisena käynnistää antioksidanttisia ja korjaavia mekanismeja

